Tóm tắt Luận án Nghiên cứu tổng hợp và tính chất của một số hợp chất 1,2,3-Triazole có chứa đồng thời vòng isatin và hợp phần monosaccharide bằng phản ứng click

Trang 1

Trang 2

Trang 3

Trang 4
Trang 5
Trang 6

Trang 7

Trang 8
Trang 9
Trang 10
Tải về để xem bản đầy đủ
Bạn đang xem 10 trang mẫu của tài liệu "Tóm tắt Luận án Nghiên cứu tổng hợp và tính chất của một số hợp chất 1,2,3-Triazole có chứa đồng thời vòng isatin và hợp phần monosaccharide bằng phản ứng click", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Tóm tắt Luận án Nghiên cứu tổng hợp và tính chất của một số hợp chất 1,2,3-Triazole có chứa đồng thời vòng isatin và hợp phần monosaccharide bằng phản ứng click

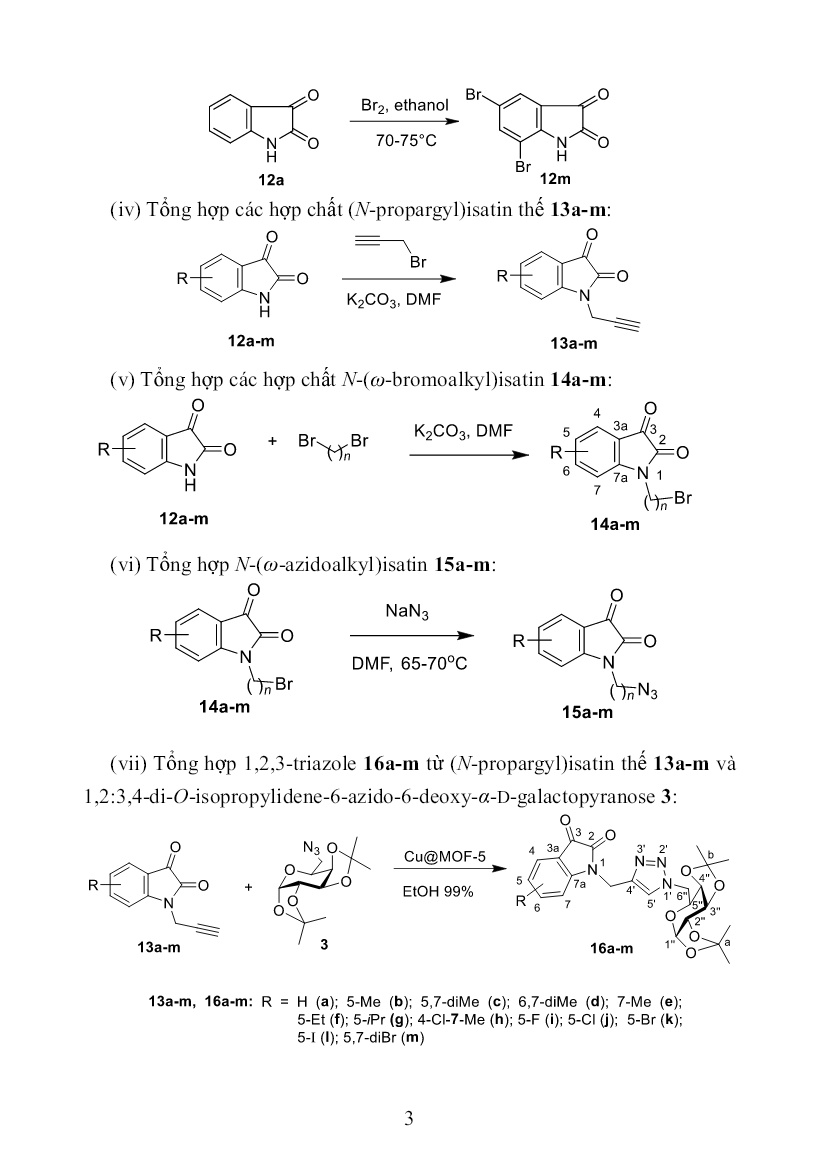
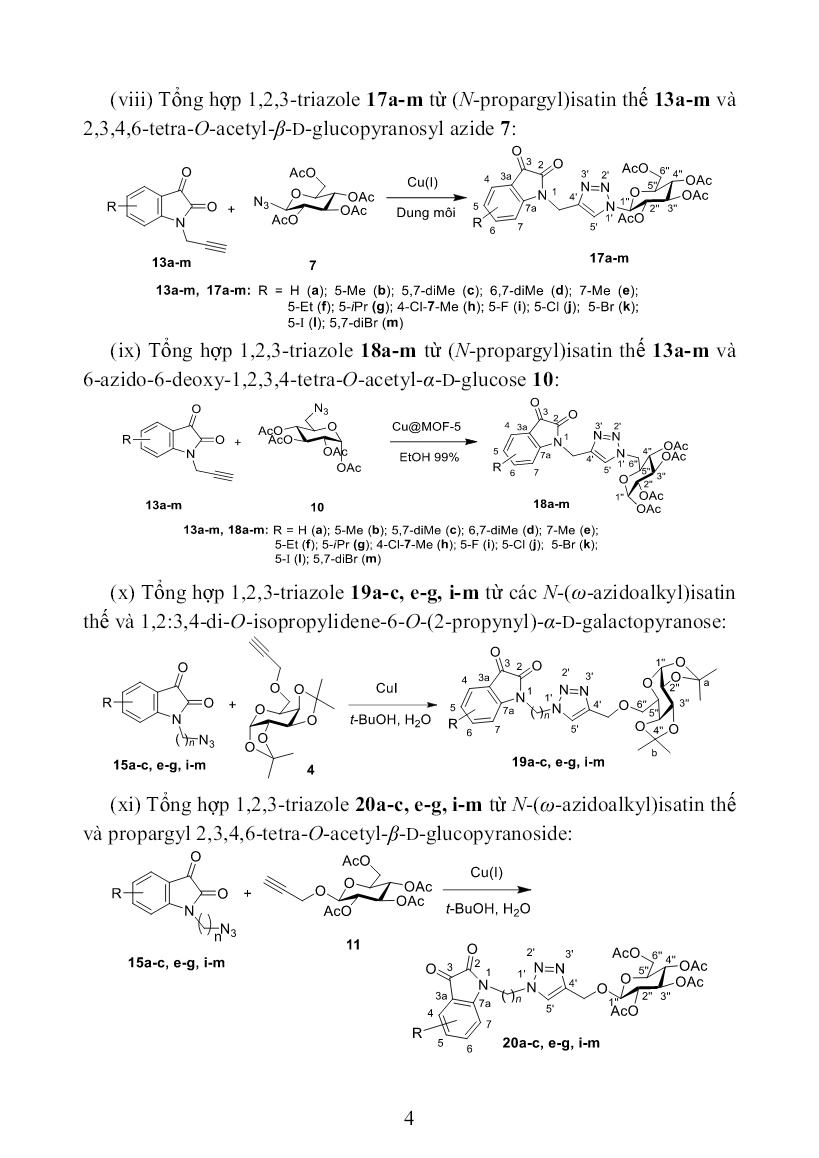
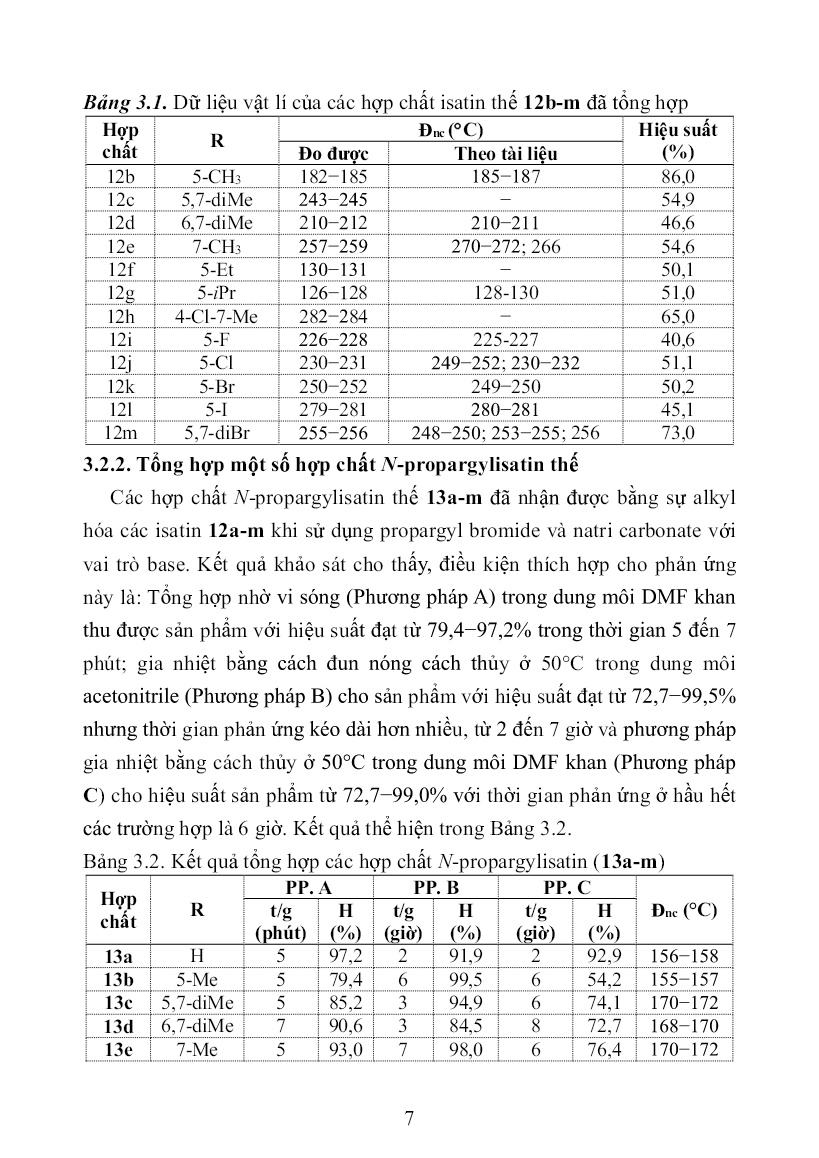
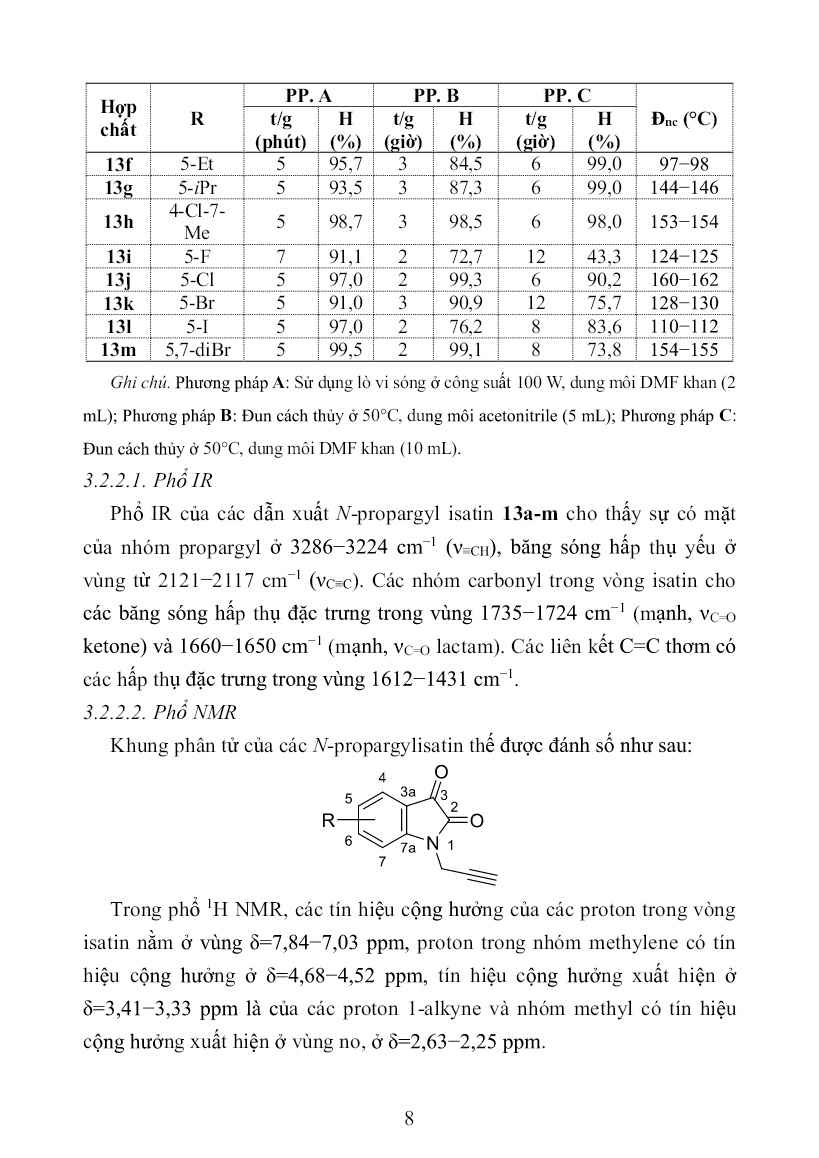
ể, màu trắng. Đnc: 114-115 oC. IR (KBr), ν (cm-1): 3277 (ν≡C−H), 2956 và 2873 (νCH alkane), 1732 (νC=O ester), 1209 và 1033 (νC-O-C ester), 2119 (νC≡C). 3.2. Tổng hợp một số dẫn xuất 1-alkyne và azido của các isatin thế 3.2.1. Tổng hợp các hợp chất isatin thế Trừ trường hợp isatin không thế (12a) có sẵn trên thị trường, các isatin thế khác (12b-l) được tổng hợp theo phương pháp Sandmeyer từ các aniline thế tương ứng hoặc bằng phản ứng thế electrophile vào vòng thơm (12m). Vì các isatin thế là chất cũ, chúng tôi chỉ tiến hành tính hiệu suất và đo điểm nóng chảy và so sánh với tài liệu tham khảo. Kết quả tổng hợp các isatin thế được thể hiện trong Bảng 3.1. 7 Bảng 3.1. Dữ liệu vật lí của các hợp chất isatin thế 12b-m đã tổng hợp Hợp chất R Đnc (C) Hiệu suất (%) Đo được Theo tài liệu 12b 5-CH3 182−185 185−187 86,0 12c 5,7-diMe 243−245 − 54,9 12d 6,7-diMe 210−212 210−211 46,6 12e 7-CH3 257−259 270−272; 266 54,6 12f 5-Et 130−131 − 50,1 12g 5-iPr 126−128 128-130 51,0 12h 4-Cl-7-Me 282−284 − 65,0 12i 5-F 226−228 225-227 40,6 12j 5-Cl 230−231 249−252; 230−232 51,1 12k 5-Br 250−252 249−250 50,2 12l 5-I 279−281 280−281 45,1 12m 5,7-diBr 255−256 248−250; 253−255; 256 73,0 3.2.2. Tổng hợp một số hợp chất N-propargylisatin thế Các hợp chất N-propargylisatin thế 13a-m đã nhận được bằng sự alkyl hóa các isatin 12a-m khi sử dụng propargyl bromide và natri carbonate với vai trò base. Kết quả khảo sát cho thấy, điều kiện thích hợp cho phản ứng này là: Tổng hợp nhờ vi sóng (Phương pháp A) trong dung môi DMF khan thu được sản phẩm với hiệu suất đạt từ 79,4−97,2% trong thời gian 5 đến 7 phút; gia nhiệt bằng cách đun nóng cách thủy ở 50°C trong dung môi acetonitrile (Phương pháp B) cho sản phẩm với hiệu suất đạt từ 72,7−99,5% nhưng thời gian phản ứng kéo dài hơn nhiều, từ 2 đến 7 giờ và phương pháp gia nhiệt bằng cách thủy ở 50°C trong dung môi DMF khan (Phương pháp C) cho hiệu suất sản phẩm từ 72,7−99,0% với thời gian phản ứng ở hầu hết các trường hợp là 6 giờ. Kết quả thể hiện trong Bảng 3.2. Bảng 3.2. Kết quả tổng hợp các hợp chất N-propargylisatin (13a-m) Hợp chất R PP. A PP. B PP. C Đnc (°C) t/g (phút) H (%) t/g (giờ) H (%) t/g (giờ) H (%) 13a H 5 97,2 2 91,9 2 92,9 156−158 13b 5-Me 5 79,4 6 99,5 6 54,2 155−157 13c 5,7-diMe 5 85,2 3 94,9 6 74,1 170−172 13d 6,7-diMe 7 90,6 3 84,5 8 72,7 168−170 13e 7-Me 5 93,0 7 98,0 6 76,4 170−172 8 Hợp chất R PP. A PP. B PP. C Đnc (°C) t/g (phút) H (%) t/g (giờ) H (%) t/g (giờ) H (%) 13f 5-Et 5 95,7 3 84,5 6 99,0 97−98 13g 5-iPr 5 93,5 3 87,3 6 99,0 144−146 13h 4-Cl-7- Me 5 98,7 3 98,5 6 98,0 153−154 13i 5-F 7 91,1 2 72,7 12 43,3 124−125 13j 5-Cl 5 97,0 2 99,3 6 90,2 160−162 13k 5-Br 5 91,0 3 90,9 12 75,7 128−130 13l 5-I 5 97,0 2 76,2 8 83,6 110−112 13m 5,7-diBr 5 99,5 2 99,1 8 73,8 154−155 Ghi chú. Phương pháp A: Sử dụng lò vi sóng ở công suất 100 W, dung môi DMF khan (2 mL); Phương pháp B: Đun cách thủy ở 50°C, dung môi acetonitrile (5 mL); Phương pháp C: Đun cách thủy ở 50°C, dung môi DMF khan (10 mL). 3.2.2.1. Phổ IR Phổ IR của các dẫn xuất N-propargyl isatin 13a-m cho thấy sự có mặt của nhóm propargyl ở 3286−3224 cm−1 (ν≡CH), băng sóng hấp thụ yếu ở vùng từ 2121−2117 cm−1 (νC≡C). Các nhóm carbonyl trong vòng isatin cho các băng sóng hấp thụ đặc trưng trong vùng 1735−1724 cm−1 (mạnh, νC=O ketone) và 1660−1650 cm−1 (mạnh, νC=O lactam). Các liên kết C=C thơm có các hấp thụ đặc trưng trong vùng 1612−1431 cm−1. 3.2.2.2. Phổ NMR Khung phân tử của các N-propargylisatin thế được đánh số như sau: Trong phổ 1H NMR, các tín hiệu cộng hưởng của các proton trong vòng isatin nằm ở vùng δ=7,84−7,03 ppm, proton trong nhóm methylene có tín hiệu cộng hưởng ở δ=4,68−4,52 ppm, tín hiệu cộng hưởng xuất hiện ở δ=3,41−3,33 ppm là của các proton 1-alkyne và nhóm methyl có tín hiệu cộng hưởng xuất hiện ở vùng no, ở δ=2,63−2,25 ppm. 9 Phổ 13C NMR xuất hiện các tín hiệu cộng hưởng của các nguyên tử carbon có mặt trong phân tử. Nguyên tử carbon trong nhóm propargyl có độ chuyển dịch hóa học ở δ=79,3−77,0 ppm và 75,6−74,8 ppm. Độ chuyển dịch hóa học của carbon trong nhóm methylene có tín hiệu ở δ=31,9-29,0 ppm. Nhóm methyl có tín hiệu ở δ=21,5−13,3 ppm. Tín hiệu cộng hưởng của carbon trong vòng thơm ở vùng δ=110−150 ppm và tín hiệu của nhóm C=O (lactam) ở khoảng δ=157 ppm. Tín hiệu cộng hưởng của nhóm C=O ketone ở khoảng 180 ppm. 3.2.2.3. Phổ MS Trên phổ ESI-MS của các chất xuất hiện các pic ion phân tử [M+H]+ và [M+Na]+ phù hợp với kết quả tính toán theo công thức phân tử dự kiến. 3.2.3. Tổng hợp một số hợp chất N-(ω-bromoalkyl)isatin thế Các hợp chất N-(ω-bromoalkyl)isatin thế 14a-m được tổng hợp khi khảo sát các phương pháp tiến hành phản ứng khác nhau. Các kết quả khảo sát cho thấy, phương pháp phù hợp để tổng hợp các hợp chất này là phương pháp khuấy ở nhiệt độ phòng và phương pháp siêu âm ở nhiệt độ phòng. Phương pháp khuấy ở nhiệt độ phòng cho hiệu suất đạt từ 28-88% với thời gian phản ứng thông thường từ 1-3 giờ, một số trường hợp ngoại lệ có thể lên tới 48 giờ. Trong khi đó, phương pháp siêu âm cho hiệu suất đạt từ 25- 79 % với thời gian phản ứng thông thường từ 3-5 giờ. Phổ IR của một số hợp chất N-(ω-bromoalkyl)isatin 14a-m xuất hiện các băng sóng hấp thụ đặc trưng như sau: Băng sóng ở 2926-2856 cm−1 (νCH, alkane), 1739-1720 cm−1 (νC=O, ketone), 1608-1467 cm−1 (νC=C, thơm). Liên kết C=O (lactam) trong vòng isatin xuất hiện băng sóng hấp thụ ở vùng 1660-1650 cm−1, tuy nhiên băng sóng này đôi khi không xuất hiện do nó bị che bởi băng sóng hấp thụ mạnh của nhóm C=O ketone. 3.2.4. Tổng hợp một số N-(ω-azidoalkyl)isatin thế Các N-(ω-azidoalkyl)isatin thế 15a-m được tổng hợp từ các N-(ω- bromoalkyl)isatin thế thông qua phản ứng với tác nhân natri azide. Khảo sát điều kiện phản ứng cho thấy, điều kiện thích hợp để tổng hợp dãy hợp chất 10 này xuất phát từ dẫn xuất bromoalkylisatin là đun cách thủy trong khi khuấy ở 65−70°C và siêu âm hỗn hợp ở nhiệt độ 65−70°C. Một phương pháp khác dùng để tổng hợp dãy hợp chất này cho kết quả rất khả quan đó là phản ứng one-pot (được thực hiện với sự trợ giúp của vi sóng ở công suất 180 W trong 7 phút, sản phẩm của bước này không được phân lập mà tiếp tục được cho phản ứng với natri azide cũng dưới các điều kiện chiếu xạ vi sóng trong 5 phút nữa ở công suất 180 W) và phản ứng theo kiểu nhiều thành phần (cho hiệu suất cao hơn nhiều so với hiệu suất ở phương pháp one-pot, tuy thời gian phản ứng một số trường hợp có dài hơn (12 phút so với 11−16 phút tương ứng)). 3.2.4.1. Phổ IR Phổ IR của N-(ω-azidoalkyl)isatin xuất hiện băng sóng hấp thụ đặc trưng như sau: Băng sóng ở vùng 2929−2872 cm−1 (νC−H, alkane), 2098 cm−1 (νN≡N, azide), 1737 cm−1 (νC=O, ketone), 1622−1491 cm−1 (νC=C, thơm). Liên kết C=O (lactam) trong vòng isatin thường cho băng sóng hấp thụ ở vùng 1660−1650 cm−1, tuy nhiên băng sóng này đôi khi không xuất hiện do nó bị che khuất bởi băng sóng hấp thụ mạnh hơn của nhóm C=O ketone. 3.2.4.2. Phổ NMR Trên phổ 1H NMR của chất đại diện 15b4 xuất hiện các tín hiệu cộng hưởng như sau: =7,63 ppm (t; J=7,75 Hz; 1H, H-6); 7,49 ppm (d; J=7,5 Hz; 1H, H-4); 7,14 ppm (d; J=8,0 Hz; 1H, H-7); 7,09 ppm (t; J=7,5 Hz; 1H, H-5); 3,64 (t; J=7,0 Hz; 2H; NCH2-); 3,46-3,43 (m; 2H; -CH2N3); 1,76 (quintet; J=7,25 Hz; 2H; NCH2CH2-); 1,61 (quintet; J=7,5 Hz; 2H; - CH2CH2N3); 1,42-1,32 (m; 4H; NCH2CH2(CH2)2CH2CH2N3). Phổ 13C NMR xuất hiện tín hiệu cộng hưởng ở trường yếu nhất thuộc về carbon C-3 (δ=183,3 ppm). Tín hiệu cộng hưởng của C-2 (nhóm chức lactam) xuất hiện ở δ=157,8 ppm. Tín hiệu cộng hưởng của carbon trong vòng thơm được qui kết như sau: δ=150,6 ppm (C-7a); 138,1 ppm (C-5); 124,3 ppm (C-7); 123,0 ppm (C-6); 117,2 ppm (C-3a); 110,5 ppm (C-4); Nguyên tử carbon còn lại được quy gán như sau: δ=34,7 (NCH2-); 32,1 (- 11 CH2N3); 27,1 ppm (NCH2CH2-); 26,5 ppm (-CH2CH2N3); 25,3 ppm (NCH2 CH2(CH2)2CH2CH2N3). 3.3. Tổng hợp các hợp chất lai 1,2,3-triazole−isatin từ các N- propargylisatin thế và 1,2:3,4-di-O-isopropylidene-6-azido-6-deoxy-α-D- galactopyranose Các hợp chất N-propargylisatin thế 13a-m đã được sử dụng làm chất đầu 1-alkyne để tổng hợp các hợp chất lai chứa dị vòng 1,2,3-triazole và isatin 16a-m trong phản ứng với 1,2:3,4-di-O-isopropylidene-6-azido-6-deoxy-α- D-galactopyranose 3 thông qua phản ứng click. Kết quả khảo sát điều kiện phản ứng cho thấy, đun cách thủy là thích hợp nhất để tổng hợp các hợp chất 1,2,3-triazole 16a-m, khi có mặt của chất xúc tác Cu@MOF-5 trong dung môi ethanol tuyệt đối ở khoảng nhiệt độ 75−80°C trong 6 giờ. Bảng 3.3. Dữ liệu tổng hợp các hợp chất 1,2,3-triazole 16a-m TT Hợp chất R Thời gian phản ứng (giờ) Đnc (°C) Hiệu suất (%) 1 16a H 6 128-130 94 2 16b 5-Me 6 117-118 76 3 16c 5,7-diMe 6 118-120 86 4 16d 6,7-diMe 6 110-111 74 5 16e 7-Me 6 140-142 98 6 16f 5-Et 6 112-114 98 7 16g 5-iPr 6 98-100 95 8 16h 4-Cl-7-Me 6 119-120 93 9 16i 5-F 6 60-62 72 10 16j 5-Cl 6 138-140 84 11 16k 5-Br 6 140-142 97 12 16l 5-I 6 130-131 80 13 16m 5,7-diBr 6 132-133 31 3.3.1. Phổ IR Phổ IR của chất 16d được ghi đại diện cho dãy. Các băng sóng hấp thụ đặc trưng bao gồm: 2983, 2922 và 2852 cm−1 (νC−H alkane); 1730 cm−1 (νC=O ketone); 1606 cm−1 (νC=O lactam); 1602, 1452 cm−1 (νC=C thơm). Các liên kết C−O−C ở acetonide và ở nhóm chức ester có các hấp thụ bị chồng chất ở 1062 và 1001 cm−1, thuộc về dao động hóa trị bất đối xứng và đối 12 xứng của liên kết này. Đặc biệt, các hấp thụ ở vùng 3286−3224 cm−1 (mạnh, ν≡CH), 2121−2117 cm−1 (yếu, νC≡C), cũng như ở 2102 cm−1 (mạnh, νN=N=N azide) không có mặt trong phổ của hợp chất 16d cũng đã xác nhận sự tạo thành của sản phẩm này. 3.3.2. Phổ NMR Khung phân tử của hợp chất 16a-m được đánh số như sau: Các tín hiệu cộng hưởng proton và carbon-13 được qui kết dựa vào phân tích phổ của hợp chất đại diện 16d. Proton H-5ʹ trong vòng 1H-1,2,3- triazole có tín hiệu cộng hưởng nằm ở trường thấp của phổ 1H NMR, với δ=8,09 ppm (ở dạng singlet), do ảnh hưởng của âm điện mạnh của nguyên tử nitơ và ảnh hưởng của hiệu ứng anisotropic của dị vòng thơm 1,2,3- triazole. Hai tín hiệu cộng hưởng ở δ=7,34 ppm và δ=7,00 ppm được quy gán lần lượt cho proton trong nhóm H-4 và H-5 của vòng isatin. Các proton của phần đường có tín hiệu trong vùng từ δ=5,35-4,09 ppm. Các proton của phần alkyl xuất hiện tín hiệu ở khoảng δ=2,51-1,20 ppm. Trên phổ 13C NMR, tín hiệu cộng hưởng ở trường yếu nhất δ=182,9 ppm được quy kết cho nguyên tử carbon C-3 (C=O ester) và tín hiệu ở δ=159,9 ppm được quy kết cho nguyên tử C-2 (lactam). Các nguyên tử carbon của phần thơm có tín hiệu ở khoảng δ=150,3-117,4 ppm. Carbon bậc 4 ở vị trí C-a và C-b xuất hiện tín hiệu lần lượt ở δ=108,8 ppm và δ=108,0 ppm. Các nguyên tử carbon trong vòng đường xuất hiện tín hiệu ở vùng δ=95,4-50,1 ppm. Các nguyên tử carbon của phần alkyl xuất hiện tín hiệu ở vùng δ=38,0-13,4 ppm. 13 Việc quy gán các proton và nguyên tử carbon dựa trên việc phân tích dữ liệu phổ COSY, HSQC và HMBC. Dưới đây là một phần phổ HSQC và HMBC của hợp chất đại diện 16d. Hình 3.1. Phổ HSQC của hợp chất 16d Hình 3.2. Phổ HMBC của hợp chất 16d 3.3.3. Phổ MS Trên phổ ESI-MS của chất đại diện 16d xuất hiện pic ion “giả phân tử” [M+H] ở số khối m/z = 499,1 phù hợp với giá trị tính toán của trọng lượng phân tử, M+H=499,21 Da, đối với công thức phân tử tương ứng C25H31N4O7 với M(tính toán)=498,21 Da. 14 3.4. Tổng hợp các hợp chất lai 1,2,3-triazole−isatin từ các N- propargylisatin thế và 2,3,4,6-tetra-O-acetyl-β-D-glucopyranosyl azide Các hợp chất lai 1,2,3-triazole 17a-m đã được tổng hợp thông qua hoá học click của N-propargyl isatin thế 13a-m với 2,3,4,6-tetra-O-acetyl-β-D- glucopyranosyl azide 7. Kết quả khảo sát cho thấy điều kiện thích hợp cho hoá học click của dãy này là đun cách thủy, sử dụng chất xúc tác CuI trong hệ dung môi t-BuOH:H2O với tỉ lệ 50:1 (về thể tích), ở nhiệt độ 75−80°C. Bảng 3.4. Dữ liệu tổng hợp các hợp chất 1,2,3-triazole 17a-m STT Hợp chất R Thời gian (giờ) Đnc (°C) Hiệu suất (%) 1 17a H 6 203−204 86 2 17b 5-Me 6 210−211 73 3 17c 5,7-diMe 6 172−173 76 4 17d 6,7-diMe 6 198−200 75 5 17e 7-Me 6 188−189 60 6 17f 5-Et 6 176−178 72 7 17g 5-iPr 6 180-182 68 8 17h 4-Cl-7-Me 6 119−120 65 9 17i 5-F 6 212−214 58 10 17j 5-Cl 6 228−229 69 11 17k 5-Br 6 241−242 65 12 17l 5-I 6 230−232 68 13 17m 5,7-diBr 6 251−252 70 Cấu trúc của các hợp chất lai 1,2,3-triazole−isatin 17a-m theo sự tổng hợp định hướng được xác nhận bằng các phương pháp phổ IR, NMR, MS. 3.4.1. Phổ IR Phổ IR xuất hiện một số băng sóng đặc trưng, bao gồm: Băng sóng hấp thụ mạnh trong vùng 1737−1734 cm−1 (νC=O, ester), 1224−1215 cm−1 và 1037−1031 cm−1 (νC−O−C, ester), 1606−1465 cm−1 (νC=C, thơm). Đặc biệt, các băng sóng hấp thụ ở vùng 2100−2200 cm−1 (thuộc về liên kết N=N=N và C≡CH) đã biến mất, điều này xác nhận sự tạo thành sản phẩm. 3.4.2. Phổ NMR Khung phân tử của hợp chất 1,2,3-triazole 17a-m được đánh số như sau: 15 Xét hợp chất đại diện 17a. Proton H-5ʹ trong vòng 1H-1,2,3-triazole nằm ở trường thấp với δ=8,47 ppm. Tín hiệu cộng hưởng của 4 proton của vòng isatin nằm trong vùng δ=7,62-7,07 ppm. Các proton của phần đường có tín hiệu trong vùng từ δ=6,31-4,06 ppm. Các proton trong nhóm methyl (acetyl) xuất hiện tín hiệu ở vùng δ=2,01-1,68 ppm. Trên phổ 13C NMR, tín hiệu cộng hưởng ở trường yếu nhất δ=182,9 ppm được quy kết cho nguyên tử carbon C-3 (C=O ester) và tín hiệu ở δ=157,7 ppm là của C-2. 4 nguyên tử carbon trong nhóm C=O (acetyl) có tín hiệu cộng hưởng xuất hiện ở vùng δ=169,9-168,2 ppm. Các nguyên tử carbon của phần thơm có tín hiệu ở δ=149,9-111,0 ppm. Các nguyên tử carbon trong vòng đường có tín hiệu ở δ=83,7-61,6 ppm. Nguyên tử carbon nhóm CH2-N và methyl (acetyl) có tín hiệu ở δ=34,9 ppm và δ=20,4-19,6 ppm. Việc quy gán các proton và nguyên tử carbon dựa trên việc phân tích dữ liệu phổ COSY, HSQC và HMBC như dưới đây. Một phần dữ liệu HSQC và HMBC thể hiện trong hình dưới đây. 3.4.3. Phổ MS Phổ ESI-MS của hợp chất đại diện 17a xuất hiện các pic ion “giả phân tử” [M+H]+ và [M+Na]+ với số khối m/z 558,92 và 581,02 hoàn toàn phù hợp với giá trị trọng lượng phân tử tương ứng với công thức phân tử C25H26N4O11, với M(tính toán)=558,16 Da. Hình 3.3. Phổ HSQC của hợp chất đại diện 17a 16 Hình 3.4. Phổ HMBC của hợp chất 17a 3.5. Tổng hợp các hợp chất 1,2,3-triazole−isatin từ N-propargylisatin thế và 6-azido-6-deoxy-1,2,3,4-tetra-O-acetyl-α-D-glucose Dựa trên những kết quả khảo sát điều kiện phản ứng, các 1,2,3-triazole 18a-m được tổng hợp từ các N-propargylisatin và 6-azido-6-deoxy-1,2,3,4- tetra-O-acetyl-α-D-glucose sử dụng xúc tác Cu@MOF-5 trong dung môi ethanol tuyệt đối bằng phương pháp đun cách thủy ở 75-80 oC. Bảng 3.5. Kết quả tổng hợp các hợp chất lai 1,2,3-triazole−isatin 18a-m STT Hợp chất R Thời gian (giờ) Đnc (°C) Hiệu suất (%) 1 18a H 8 133−135 49 2 18b 5-Me 10 142−144 63 3 18c 5,7-diMe 10 125−127 41 4 18d 6,7-diMe 8 154−156 36 5 18e 7-Me 9 168−170 52 6 18f 5-Et 7 122−124 44 7 18g 5-iC3H7 9 156−158 52 8 18h 4-Cl-7-Me 12 146-148 54 9 18i 5-F 8 182−184 65 10 18j 5-Cl 10 198−200 62 11 18k 5-Br 8 210−212 31 12 18l 5-I 9 204−206 44 13 18m 5,7-diBr 7 228−230 73 3.5.1. Phổ IR Phổ IR xuất hiện một số băng sóng đặc trưng, bao gồm: Băng sóng hấp thụ ở 3134 cm−1 và 2981 cm−1 là của dao động hóa trị của liên kết C−H (thơm) và C−H (alkane), 1734 cm−1 (νC=O, ester), 1211 cm−1 và 1029 cm−1 (νC−O−C, ester), 1620 cm-1 và 1489 cm−1 (νC=C, thơm). 17 3.5.2. Phổ NMR Khung phân tử của các hợp chất 18 được đánh số như sau: Xét hợp chất đại diện 18f, tín hiệu cộng hưởng xuất hiện ở trường yếu nhất tại δ=8,09 ppm (s, 1H) được qui kết cho proton ở vị trí H-5ʹ. Tín hiệu cộng hưởng của các proton trong vòng isatin xuất hiện ở δ=7,47−7,02 ppm. Các proton của vòng đường có độ chuyển dịch hóa học ở vùng δ=6,05-4,34 ppm và các proton alkyl có tín hiệu xuất hiện ở δ=2,59-1,15 ppm. Trên phổ 13C NMR, tín hiệu cộng hưởng ở trường yếu nhất δ=183,3 ppm được quy kết cho nguyên tử carbon C-3 (C=O ester) và tín hiệu ở δ=157,8 ppm được quy kết cho nguyên tử C-2 (lactam). 4 nguyên tử carbon trong nhóm C=O (acetyl) có tín hiệu cộng hưởng xuất hiện ở vùng δ=169,6-168,7 ppm. Các nguyên tử carbon của phần thơm có tín hiệu nằm ở khoảng δ=148,2-111,1 ppm. Các nguyên tử carbon trong vòng đường có tín hiệu ở vùng δ=87,9-49,6 ppm và các nguyên tử carbon trong hợp phần alkyl có tín hiệu ở vùng δ=39,1-15,5 ppm. Một phần dữ liệu phổ HSQC và HMBC thể hiện trong hình dưới đây. Hình 3.5. Phổ HSQC của hợp chất 18f 18 Hình 3.6. Phổ HMBC của hợp chất 18f 3.5.3. Phổ MS Phổ ESI-MS của hợp chất 18f xuất hiện pic ion “giả phân tử” [M+H]+ có số khối m/z 587,1 là hoàn toàn phù hợp với giá trị trọng lượng phân tử tương ứng với công thức phân tử C27H30N4O11, với M(tính toán)=586,2 Da. 3.6. Tổng hợp các hợp chất lai 1,2,3-triazole−isatin từ các N-(ω- azidoalkyl)-isatin thế và 1,2:3,4-di-O-isopropylidene-6-O-(2-propynyl)- α-D-galactopyranose Các hợp chất lai 1,2,3-triazole−isatin 19a-c,e-g,i-m được tổng hợp từ các N-(ω-azidoalkyl)isatin 15a-c,e-g,i-m với hợp phần 1,2:3,4-di-O- isopropylidene-6-O-(2-propynyl)-α-D-galactopyranose 4 thông qua phản ứng click. Dựa trên kết quả khảo sát điều kiện phản ứng, phương pháp tối ưu là đun cách thủy ở khoảng nhiệt độ 75−80°C trong sự có mặt của các chất xúc tác CuI, dung môi t-BuOH/H2O. Hiệu suất của phản ứng đạt từ 34- 96% trong thời gian từ 6-19 giờ. 3.6.1. Phổ IR Phổ IR của hợp chất đại diện 19b4 xuất hiện băng sóng hấp thụ ở 2983, 2922 và 2856 cm−1 (νC–H, alkane), 1730 cm−1 (νC=O ester), 1211 và 1064 cm−1 (νC−O−C ester), 1622, 1600, 1490 cm−1 (νC=C thơm). Đặc biệt, các băng sóng hấp thụ ở vùng 2100−2200 cm−1 (thuộc về liên kết N=N=N và C≡CH) đã biến mất, điều này xác nhận sự tạo thành sản phẩm. 19 3.6.2. Phổ NMR Khung phân tử của các hợp chất 19a-c,e-g,i-m được đánh số như sau: Trên phổ 1H NMR của chất đại diện 19b4 tín hiệu xuất hiện ở trường yếu nhất δ=8,07 ppm (s, 1H) được qui kết cho proton H-5ʹ vòng 1,2,3-triazole. Tín hiệu cộng hưởng của các proton trong vòng isatin xuất hiện ở vùng δ=7,45−7,06 ppm. Các proton của vòng đường có độ chuyển dịch hóa học ở δ=5,44-3,45 ppm, các proton alkyl có tín hiệu xuất hiện ở δ=2,50-1,27 ppm. Trên phổ 13C NMR, tín hiệu cộng hưởng ở trường yếu nhất δ=183,6 ppm được quy kết cho nguyên tử carbon C-3 (C=O ester) và tín hiệu ở δ=158,2 ppm được quy kết cho nguyên tử C-2 (lactam). Các nguyên tử carbon của phần thơm có tín hiệu nằm ở khoảng δ=148,4-110,4 ppm. Các nguyên tử carbon trong vòng đường có tín hiệu ở vùng δ=95,6-63,6 ppm. Các nguyên tử carbon trong hợp phần alkyl có tín hiệu ở vùng δ=48,8-20,0 ppm. 3.6.3. Phổ MS Phổ ESI-MS của hợp chất 19b4 xuất hiện pic ion “giả phân tử” [M+H]+ có số khối m/z 557,1 là hoàn toàn phù hợp với giá trị trọng lượng phân tử tương ứng với công thức phân tử C28H36N4O8, với M(tính toán)=556,2 Da. Hình 3.7. Phổ HSQC của hợp chất 19b4 20 Hình 3.8. Phổ HMBC của hợp chất 19b4 (vùng thơm) Hình 3.9. Phổ HMBC của hợp chất 19b4 (vùng đường) 3.7. Tổng hợp các hợp chất lai 1,2,3-triazole−isatin từ các N-(ω- azidoalkyl)-isatin thế và propargyl 2,3,4,6-tetra-O-acetyl-β-D- glucopyranoside Các 1,2,3-triazole 20a-c,e-g,i-m được tổng hợp từ các N-(ω- azidoalkyl)isatin 14a-c,e-g,i-m với hợp phần propargyl 2,3,4,6-tetra-O- acetyl-β-D-glucopyranoside 8 thông qua phản ứng click. Điều kiện phản ứng thích hợp là đun nóng cách thủy ở nhiệt độ 75−80°C, xúc tác Cu0/Mont-K10, hệ dung môi t-BuOH/H2O tỉ lệ 50:1 (về thể tích). Hiệu suất đạt được từ 62-98% với thời gian phản ứ
File đính kèm:
 tom_tat_luan_an_nghien_cuu_tong_hop_va_tinh_chat_cua_mot_so.pdf
tom_tat_luan_an_nghien_cuu_tong_hop_va_tinh_chat_cua_mot_so.pdf Trích yếu luận án.pdf
Trích yếu luận án.pdf Trang thông tin đóng góp mới.pdf
Trang thông tin đóng góp mới.pdf TRang thông tin đóng góp mới.doc
TRang thông tin đóng góp mới.doc Tóm tắt luận án tiếng anh.pdf
Tóm tắt luận án tiếng anh.pdf QĐ thành lập HĐ đánh giá luận án tiến sĩ cấp học viện.pdf
QĐ thành lập HĐ đánh giá luận án tiến sĩ cấp học viện.pdf

